Практическая работа
Качественное определение углерода, водорода и хлора в органических соединениях
Цели. Научиться экспериментально
доказывать качественный состав углеводородов и
их галогенопроизводных, обосновывать данные
эксперимента.
Оборудование и реактивы
. Шпатели (2 шт.),
кусочек ваты, U- и Г-образные газоотводные трубки,
газоотводная трубка-капилляр, спиртовка, спички,
штатив железный с лотком, широкогорлая пробирка,
пипетка, промывочная склянка, штатив с
пробирками, щипцы тигельные, фильтровальная
бумага, фарфоровая чашка, синее стекло (Со),
санитарная склянка, стакан на 50 мл; лакмусовая
бумага (фиолет.), С2Н5ОН (3–4 мл),
известковая вода Са(ОН)2 или баритовая вода
Ba(OH)2, парафин (измельченный), сахароза С12Н22О11,
CuO (порошок), CuSO4 (безвод.), HNO3 (конц.),
хлороформ СНСl3 или четыреххлористый
углерод CCl4, Na металлический (2–3 горошины,
свежеочищенный), AgNO3 (р-р, ![]() = 1%), Cu (тонкая проволока, на конце
скрученная в спираль).
= 1%), Cu (тонкая проволока, на конце
скрученная в спираль).
Проба Бейльштейна. При нагревании
с СuO галогенсодержащие вещества сгорают с
образованием летучих соединений меди с
галогеном, окрашивающих пламя в сине-зеленый
цвет.
Реакция Степанова
. Наличие
галогена определяют путем восстановления
соединения галогена водородом (атомарным, в
момент выделения). Галоген отщепляется в виде
галогеноводорода, обнаруживаемого реакцией с
нитратом серебра(I) по белому творожистому осадку
AgCl, нерастворимому в кислотах. Водород получают
действием металлического Na на спирт.
| Порядок работы | Задания | Наблюдения и выводы |
|---|---|---|
| 1. В
пробирке
смешать (1:3) немного сахара С12Н22О11
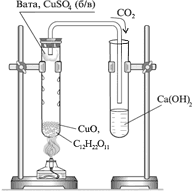
с оксидом меди(II), засыпав оксидом смесь и сверху. 2. В верхнюю часть пробирки (под пробку) поместить комок ваты, на которую насыпать немного безводной сернокислой меди(II).
|
Доказать опытным путем, что в составе выданного органического вещества имеются углерод и водород. Назвать признаки наблюдаемых химических реакций. | ... |
| 3. Пробирку закрыть пробкой с газоотводной трубкой, конец которой должен быть в сборнике над уровнем известковой воды. Нагревать сначала всю пробирку, затем смесь. Наблюдать | Написать
уравнения протекающих реакций. Дополнительно
написать уравнения реакций сжигания с CuO веществ а) CCl4; б) глюкозы С6Н12О6; в) глицерина С3Н8О3 |
... |
| Медную проволоку, взятую щипцами, прокалить в пламени горелки для образования на ее поверхности слоя оксида меди(II). Если пламя окрашивается в сине-зеленый цвет, то нагрев вести до исчезновения этой окраски. После охлаждения смочить кончик проволоки в испытываемом веществе CCl4 и ввести в несветящееся пламя | Доказать опытным путем наличие в составе четыреххлористого углерода атомов галогена. Доказательство провести двумя способами. Объяснить результаты эксперимента, записать уравнения реакций распознавания | ... |
| Демонстрационный опыт. В 2–3 мл С2Н5ОН (обезвоженного безводным CuSO4) растворить несколько капель (крупинок) испытываемого вещества и добавить кусочек металлического Na (горошину). По окончании выделения водорода, убедившись в полном растворении натрия, смесь разбавить равным объемом воды, подкислить концентрированным раствором HNO3 и прилить 1%-й раствор нитрата серебра(I) | Объяснить |